我们生物体所有器官的细胞都起源于干细胞。干细胞分裂产生的细胞可以发育成机体特定组织如形成大脑、肺或骨髓。然而,随着年龄的增长,机体内的干细胞会逐渐失去增殖分化的能力,许多干细胞会陷入了休眠状态。理解这背后的机制有助于发现对抗年龄相关疾病的方法。
来自卢森堡大学卢森堡系统生物医学中心(LCSB)和德国癌症研究中心(DKFZ)的科学家合作在国际顶级期刊 Cell 杂志在线刊发题为”Quiescence Modulates Stem Cell Maintenance and Regenerative Capacity in the Aging Brain(衰老大脑内干细胞休眠状态维持和再生能力的调控)“的研究论文。
1.干细胞休眠的发生原因
研究发现,随着年龄增加,小鼠大脑中的神经干细胞数量出现显著下降,而剩下的神经干细胞会进入休眠状态,从而保全整个神经干细胞家族不至于完全消失。
通常情况下,当大脑出现损伤,神经干细胞应该被唤醒继续工作,完成它修复大脑损伤的神圣使命。但研究发现,休眠使得这些衰老的神经干细胞很难苏醒。而进一步研究发现,这些休眠的神经干细胞一旦被激活,在增殖和分化能力方面,它们就可以和年轻神经干细胞一样朝气蓬勃。另外,年龄对神经干细胞的转录组造成的改变很小。
那么,是什么导致了休眠的发生呢?
进一步的机制研究发现,神经干细胞龛来源的炎症信号以及Wnt信号通路的拮抗剂sFRP5都可以导致休眠的发生。而在细胞稳态和受到损伤时,干扰上述炎症信号或拮抗剂的功能,均可增加这些休眠神经干细胞的激活(见下图)。
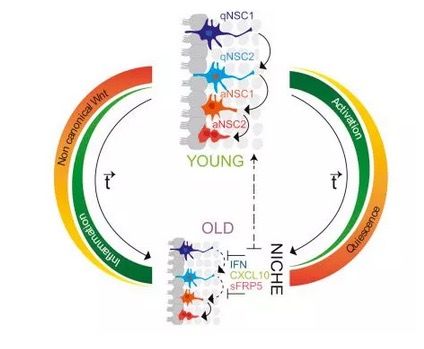
图片来源:Cell
这些神经干细胞的休眠主要由神经干细胞环境中的炎症信号介导。因此,抗炎物质也许是唤醒这些干细胞并刺激衰老大脑中的修复过程的关键所在。
2.激活休眠的神经干细胞
人类大脑中,特定部位的神经干细胞可以终生产生新的神经元,这些神经干细胞也会在大脑损伤后被激活,此外还可能成为特殊脑癌的源头。但是在衰老的大脑中,年轻神经元的补充会减少。
随着年龄的增长,休眠的神经干细胞数量会越来越多,损伤等紧急信号也使得其被唤醒的难度也越来越大。
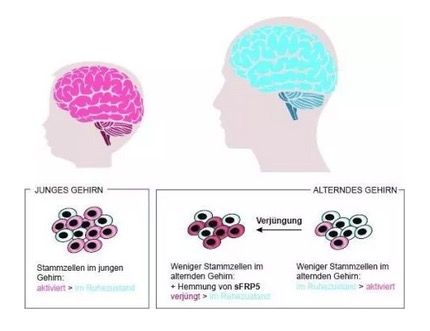
sFRP5基因失活可以促进神经干细胞活化增殖
该研究团队发现,一种叫做sFRP5的分子控制着老年小鼠的神经干细胞的休眠状态,并且sFRP5分子是通过阻断对细胞分化至关重要的Wnt通路来抑制神经干细胞增殖的。
研究结果显示:当抑制sFRP5的功能时,处于休眠的干细胞开始具有更活跃的增殖能力,使得老年小鼠大脑中活跃的干细胞与休眠的干细胞的比例几乎与年轻动物一样,并且这些活跃的干细胞可以被再次招募到老化的大脑区域,进一步行使再生修复损伤的功能。
“我们工作的核心发现是炎症促进的大脑的神经干细胞休眠,这是衰老大脑中神经干细胞的关键特点。” Martin-Villalba说道。“但是,我们可以用药物降低炎症水平,这也许是一种促进衰老大脑中神经元再生并启动神经修复机制的有效方法。”
参考文献:
Quiescence Modulates Stem Cell Maintenance and Regenerative Capacity in the Aging Brain. Cell. February 28, 2109.
