内布拉斯加州大学林肯分校(University of Nebraska-Lincoln)、威斯塔研究所(Wistar Institute)和其他研究机构合作的一项最新研究表明,锁定一扇允许能源物质进入免疫抑制细胞的生化大门,可以减缓肿瘤的进展,并有助于治疗多种癌症。
这项于近日发表在《Nature》杂志上的研究发现,在一种已知能够抑制免疫反应、阻碍癌症治疗的细胞中,脂肪酸转运蛋白2 (FATP2)水平升高。在从人类和小鼠身上分离出肿瘤细胞后,研究人员还发现,FATP2帮助产生并运输进入细胞的能量供给脂质的数量显着增加。
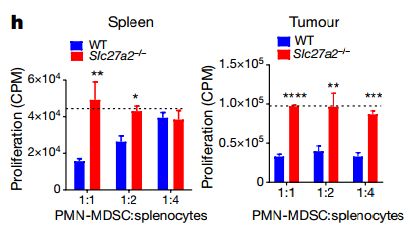
图片来源:Nature
总的来说,这项研究的结果表明,FATP2参与了对人体最常见的白细胞进行恶意重组的过程,导致这些白细胞无法在对抗感染时就会扮演第一反应者的角色。
当研究人员剔除了与FATP2相关的基因后,他们发现几种癌症--淋巴瘤、肺癌、结肠癌和胰腺癌--在小鼠体内的生长速度明显变慢。此前,内布拉斯加州的Concetta DiRusso发现了一种抑制FATP2的化合物--Lipofermata,在与一种破坏细胞复制的药物配药时,这种化合物同样有助于减缓甚至抑制肿瘤生长。研究表明,在免疫抑制细胞中靶向FATP2可以阻止脂质积聚,减轻肿瘤进展,而不会产生明显的副作用。"我认为特殊的地方在于这不是针对一种特定的癌症,这也是让我们兴奋的地方。" DiRusso是这项研究的合作者之一,也是乔治霍姆斯大学的生物化学教授。"能够针对不同癌症的一些常见细胞是一件非常令人期待的事情。"
它不能完全清除(肿瘤),但它能发挥一定的抑制效果。我们现在对联合治疗更感兴趣。它不是只针对一个目标,而是以多种方式靶向肿瘤,因为肿瘤很聪明。肿瘤找到了一种绕过我们最好的药物的方法,这就是为什么这些药物组合如此强大,我们希望,更有效。
"Wistar研究所的Dmitry Gabrilovich和他的同事们在几年前首次注意到实体肿瘤中FATP2的增加。他们的观察促使Gabrilovich联系了内布拉斯加州的生物化学家Paul Black,他研究了脂肪分子如何穿过细胞膜的基本原理。
Black的实验室对酵母的早期研究发现了一个基因片段和相关蛋白,它能激活并携带脂肪酸进入细胞,在细胞中脂肪酸代谢为能量或嵌入细胞膜。这个蛋白质正是FATP2。
Charles Bessey教授兼生物化学系主任Black说:"如果细胞膜上有一个控制进入体内的脂肪量的闸门,然后你开始控制这个闸门,它会影响下游的物质。如果一个癌细胞需要被喂以脂质才能发生转移,成为一种严重的疾病,那它就必须上调这种蛋白质的含量。所以这个门在所有这些代谢系统中扮演着非常关键的角色。"
Black之前的研究也帮助确定了FATP2有两种基因变体:一种是用于代谢的主要脂肪酸,另一种是用于跨细胞膜运输它们。这一重要区别为DiRusso实验室的研究提供了依据。该实验室筛选了超过10万种可能有助于对抗肥胖和2型糖尿病的抗FATP2化合物。
最有效的候选药物Lipofermata基本上消除了组织培养中的脂肪积累,并将小鼠对脂类的吸收降低了60%以上,这使得DiRusso获得了该药物用于治疗代谢疾病的专利。所以当Gabrilovich联系Black时,他很快就和DiRusso取得了联系。这两个人最终为Gabrilovich提供了进行他的团队实验所需的生化观点、样本和Lipofermata。
Black说:"无论是癌症生物学还是糖尿病,还是你在这个生物医学世界里追求的任何东西,你都不能再自己做了。"他说:"我们可以坐起来,做自己的事,就像一个小竖井一样,这样的日子已经一去不复返了。我们早期的一些机械工作就是这样做的,但是现在的工作太复杂了。它只是大量的信息。"我们还不知道事情的全貌,但即将公布的数据将会非常非常快地推动这件事向前发展。"
参考资料:Dmitry I. Gabrilovich et al. Fatty acid transporter 2 reprograms neutrophils in cancer, Nature (2019). DOI: 10.1038/s41586-019-1118-2
